Estrutura da matéria – Atividade 8 - 07/05/2021
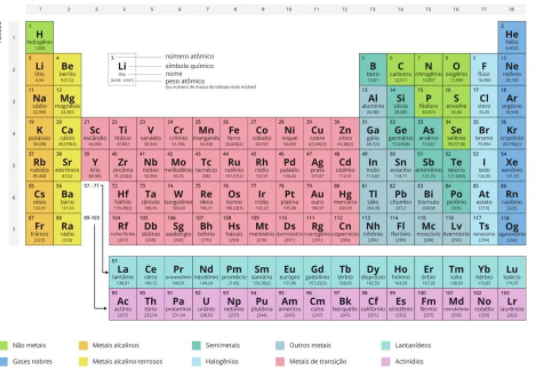
Os Principais Elementos Químicos
Você já ouviu falar em alguns elementos químicos, como o Oxigênio, Carbono, Ferro, Alumínio, Chumbo, Fósforo, entre muitos outros. Esses elementos químicos são organizados e estruturados de acordo com algumas propriedades químicas, tais como: quantidade de elétrons, raio atômico, número atômico, massa atômica e outros.
Essa organização é feita em uma tabela, hoje conhecida como tabela periódica dos elementos químicos, que foi sendo estruturada ao longo do tempo, desde os alquimistas que criavam símbolos para algumas substâncias e organizavam em tabelas, embora não houvesse um consenso ou lógica científica para essa organização. No século XVIII, o químico francês Antoine-Laurent de Lavoisier estruturou em seu livro uma organização científica para os elementos químicos, mas ainda usando alguns dos símbolos da alquimia. Até o século XIX surgiram outros esboços de organizações dos elementos químicos, quando surge a proposição do químico russo Dimitri Ivanovich Mendeleiev. Para organizar os nomes e os símbolos o químico sueco Jöns Jacob Berzelius propôs que deveriam ser descritos em latim ou grego para universalizar, tanto para os nomes quanto os símbolos que representavam, em vez de usar símbolos abstratos e nomes variados, pois podia gerar confusão.
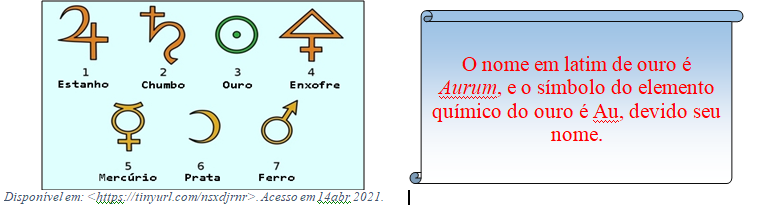
Mendeleiev propôs que os elementos químicos deveriam ser organizados de acordo com sua massa atômica, mas não apenas isso, ele afirmou que havia uma lógica entre as massas, o que poderiam ser colocadas em grupos específicos de elementos químicos. O diferencial da teoria de Mendeleiev, foi que ele deixou espaços em branco na sua tabela afirmando que mais elementos seriam descobertos indicando sua massa atômica, em uma época que apenas 62 elementos químicos eram conhecidos.
Em1869 a tabela periódica de Mendeleiev foi divulgada. No início muitos não acreditavam na teoria de Mendeleiev devido sua previsão dos novos elementos, chamados por ele de eka-boron, eka-aluminium, e eka-silicon. Conforme os anos passaram esses elementos propostos por ele foram encontrados, sendo eles Gálio, Escândio e Germânio respectivamente, e suas massas eram muito semelhantes às que ele propôs. Assim, sua teoria foi aceita.
Após a descoberta do próton e do elétron nos anos finais do século XIX, uma proposta de atualização na forma de se organizar a tabela periódica foi sugerida por Henry Moseley em 1913, usando agora a quantidade de prótons, chamada de número atômico, como referência para organização. Essa é a tabela periódica atual, organizada tanto pelo número atômico quanto pela distribuição dos elétrons, seguindo a teoria de Bohr.
A Tabela Periódica
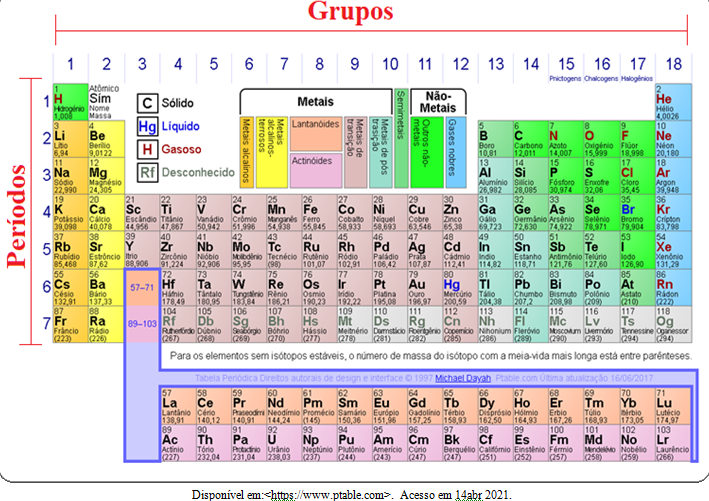
Organização periódica dos elementos químicos
A tabela periódica se divide em Períodos e Grupos (linhas e colunas), onde cada grupo tem propriedades químicas semelhantes, relação em massa e o final de sua distribuição eletrônica é o mesmo, divididas entre 1 e 18. Os períodos representam a quantidades de camadas de elétrons, como por exemplo, no período 5 existem 5 camadas de elétrons, no período 2, existem 2 camadas de elétrons. Os períodos, também representam o tamanho dos átomos, que quanto maior o período, maior o raio atômico.
Uma forma para localizar um elemento químico pode ser de feita pelas coordenadas do período e do grupo.
Exemplo1: Elemento químico: Enxofre (S)
Está localizado no Período 3, Grupo 16.

Exemplo2 :Elemento químico: Prata (Ag)
Está localizado no Período 5, Grupo 11.
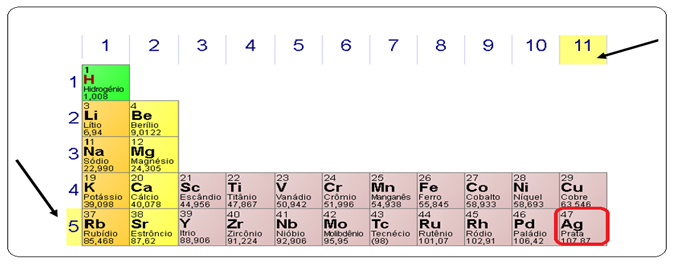
Os principais elementos químicos
A química está ligada intimamente a vida, e os principais elementos químicos presentes no corpo humano são: Oxigênio, Carbono, Hidrogênio, Nitrogênio, Cálcio, Fósforo, Potássio, Enxofre, Sódio, Cloro, Magnésio, Ferro e outros elementos químicos em quantidades muito pequenas, sendo que os quatro primeiros citados correspondem a cerca de 96% do nosso organismo.
A maioria dos elementos presentes no corpo humano estão nos três primeiros períodos da tabela periódica (1, 2 e 3), com poucas exceções, como o Potássio, o Cálcio e o Ferro. O que indica que os elementos que propiciam a vida são elementos mais leves, e o contato com alguns elementos mais pesados pode ser tóxico, como o Chumbo, o Mercúrio que estão no 6º período.
Cada elemento químico tem sua função bem definida no organismo como o oxigênio, que está presente principalmente na respiração celular e na água que compõe o corpo humano, o carbono está presente em todas as células do nosso organismo, como elemento fundamental da vida, o hidrogênio, que está sempre associado a algum outro elemento, como oxigênio na água e o carbono em todas as células, o nitrogênio é essencial para o metabolismo das células, nas proteínas conhecidas como aminoácidos, o cálcio está presente em nossa estrutura óssea e auxilia no metabolismo, o fósforo está presente nos ossos também, mas sua principal função no corpo é fornecer energia para as células.
Quer saber mais sobre a Tabela Periódica? Assista, se possível, ao vídeo.
Responda as atividades em seu caderno.
01. A tabela periódica agrupa todos os elementos químicos conhecidos e suas propriedades. Qual o período na tabela periódica que se encontram a maior quantidade de elementos químicos essenciais para a vida na terra?
02. Analisando a tabela periódica, os elementos do Período 3, Grupo 13 e Período 6, Grupo 11 são indicados, respectivamente, por:
| a) ( ) Sc e Cu. | b) ( ) O e N. | c) ( ) Au e Al. | d) ( ) Cs e Hg. |
03. Analise as afirmativas a seguir relacionadas à tabela periódica.
I – A tabela periódica atual está organizada em ordem crescente de configuração eletrônica.
II – O elemento Ferro (Fe) está presente no 4˚ período. Apresenta átomos com apenas 4 níveis e sua camada de valência é a quarta.
III – Conhecendo o período que um determinado elemento ocupa na tabela periódica, épossível identificar o número de níveis e a camada de valência do átomo.
IV – A Tabela Periódica foi proposta por Mendeleiev, em 1913, sendo organizada com base em uma ordem crescente de número atômico dos elementos químicos.
Assinale a alternativa que indica as afirmações coerentes com o tema.
| a) ( ) II e III. | b) ( ) II e IV. | c) ( ) I, II e III. | d) ( ) II, III e IV. |
04.A finalidade básica de se criar uma tabela era facilitar a classificação, a organização e o agrupamento dos elementos químicos conforme suas propriedades. Quais características os elementos presentes em um mesmo grupo têm em comum:
a) ( ) Propriedades químicas e raio atômico.
b) ( ) Quantidade de camadas e raio atômico.
c) () Relação em massa e distribuição eletrônica.
d) ( ) Distribuição eletrônica e quantidade de camadas.
05. Relacione os termos utilizados na tabela periódica.
(a) Família (b) Período (c) Lantanídeos (d) Actinídeos
(__) É uma série que possui elementos cujos números atômicos vão de 57 a 71, apresentando sempre seis níveis eletrônicos.
(__) São as linhas horizontais numeradas, que possuem elementos que apresentam o mesmo número de camadas eletrônicas.
(__) Correspondem as sequências verticais da tabela periódica, agrupados de acordo comsemelhanças em suas propriedades químicas.
(__) Formam uma série na tabela periódica com números atômicos que variam do 89 ao 103, chamados elementos de transição interna e todos os isótopos destes compostos são radioativos.
06. Determine as coordenadas de período e grupo dos seguintes elementos químicos:
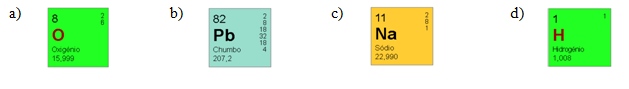
Se for possível, clique aqui para baixar ou imprimir a aula.
